보건복지부는 첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률 시행령과 시행규칙 제정안을 21일부터 다음달 31일까지 입법예고한다고 밝혔다.
제정안은 첨단재생의료 임상연구 심의·승인 절차를 마련하고 실시 의료기관 지정과 첨단바이오의약품의 신속한 제품화, 전주기 안전관리체계 마련 등의 내용을 담고 있다. 지난해 8월 국회 본회의를 통과해 올해 8월28일부터 시행할 예정이다.
시행령에는 첨단재생의료 범위를 세포치료, 유전자치료, 조직공학치료, 융복합치료 4개로 분류하고 임상연구 위험도를 고, 중, 저로 구분하고 최종 심의위원회 결정사항으로 규정했다.
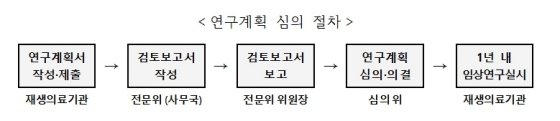
심의위원회는 재생의료기관의 연구계획 적합여부를 심의하고 연구 결과보고, 연구계획 변경, 이상 발생시 연구중단·중지·재개 여부 등을 결정하게 된다. 위원회별 10명 안팎의 민간전문가로 구성된 전문위원회를 유형별 4개로 두고 연구계획, 유효성·안전성 검증을 진행한다. 보건복지부와 식품의약품안전처는 공동 사무국을 설치해 행정과 사무 지원을 하게 된다.
 |
총리령으로 제정되는 첨단바이오의약품 안전 및 지원에 관한 규칙으로는 △세포처리시설 및 인체세포등관리업 허가 절차 등 규정 △첨단바이오의약품 제조업 허가・품목허가 갱신 등 규정 △장기추적조사 계획 수립・준수사항 규정 첨단바이오의약품 품목 분류 △신속허가를 위한 대상 지정 및 맞춤형 심사・조건부허가 도입 등이 담겼다.
특히 코로나19(신종 코로나바이러스감염증)처럼 대체치료제가 없고 생명을 위협하는 중대한 질환이나 희귀질환, 감염병 대유행 예방 치료 등을 목적으로 하는 의약품을 신속처리대상으로 지정하는 절차를 규정하는 내용도 담겼다. 개발자 일정에 맞춰 허가자료를 미리 제출받는 사전심사와 종전 115일이 걸리는 심사를 90일로 줄인 우선심사, 희귀질환 등에 대해선 3상을 의약품 시판후 시행하는 조건으로 2상 자료로 허가하는 조건부 허가 등의 지원체계가 마련된다.
아울러 시행규칙에서는 △재생의료기관 지정·관리 △세포처리시설장의 준수의무 규정 △안전관리기관 지정 및 업무수행 절차 규정 등이 담겼다.
보건복지부와 식품의약품안전처는 이번 제정안에 대해 의견이 있는 단체나 개인은 입법예고기간 보건복지부 보건의료기술개발과 식품의약품안전처 바이오의약품정책과, 국민참여입법센터로 의견을 제출해 달라고 당부했다.
제정안에 대한 상세한 사항은 보건복지부 누리집(www.mohw.go.kr), 식품의약품안전처 누리집(www.mfds.go.kr), 국민참여입법센터(opnion.lawmaking.go.kr)에서 확인할 수 있다.





 신고
신고 인쇄
인쇄 스크랩
스크랩











